Если у плода порок сердца что делать. Закономерности изменений показателей ультразвукового исследования при врожденных пороках сердца у плода в зависимости от особенностей внутрисердечной гемодинамики антенатального периода
– группа заболеваний, объединенных наличием анатомических дефектов сердца, его клапанного аппарата или сосудов, возникших во внутриутробном периоде, приводящих к изменению внутрисердечной и системной гемодинамики. Проявления врожденного порока сердца зависят от его вида; к наиболее характерным симптомам относятся бледность или синюшность кожных покровов, шумы в сердце, отставание в физическом развитии, признаки дыхательной и сердечной недостаточности. При подозрении на врожденный порок сердца выполняется ЭКГ, ФКГ, рентгенография, ЭхоКГ, катетеризация сердца и аортография, кардиография, МРТ сердца и т. д. Чаще всего при врожденных пороках сердца прибегают к кардиохирургической операции – оперативной коррекции выявленной аномалии.
Осложнениями врожденных пороков сердца могут стать бактериальный эндокардит , полицитемия , тромбозы периферических сосудов и тромбоэмболии сосудов головного мозга, застойные пневмонии , синкопальные состояния , одышечно-цианотические приступы, стенокардитический синдром или инфаркт миокарда .
Диагностика врожденных пороков сердца
Выявление врожденных пороков сердца осуществляется путем комплексного обследования. При осмотре ребенка отмечают окраску кожных покровов: наличие или отсутствие цианоза, его характер (периферический, генерализованный). При аускультации сердца нередко выявляется изменение (ослабление, усиление или расщепление) сердечных тонов, наличие шумов и пр. Физикальное обследование при подозрении на врожденный порок сердца дополняется инструментальной диагностикой - электрокардиографией (ЭКГ), фонокардиографией (ФКГ), рентгенографией органов грудной клетки , эхокардиографией (ЭхоКГ).
ЭКГ позволяет выявить гипертрофию различных отделов сердца, патологическое отклонение ЭОС, наличие аритмий и нарушений проводимости, что в совокупности с данными других методов клинического обследования позволяет судить о тяжести врожденного порока сердца. С помощью суточного холтеровского ЭКГ-мониторирования обнаруживаются скрытые нарушения ритма и проводимости. Посредством ФКГ более тщательно и детально оценивается характер, длительность и локализация сердечных тонов и шумов. Данные рентгенографии органов грудной клетки дополняют предыдущие методы за счет оценки состояния малого круга кровообращения, расположения, формы и размеров сердца, изменений со стороны других органов (легких, плевры, позвоночника). При проведении ЭхоКГ визуализируются анатомические дефекты перегородок и клапанов сердца, расположение магистральных сосудов, оценивается сократительная способность миокарда.
При сложных врожденных пороках сердца, а также сопутствующей легочной гипертензии, с целью точной анатомической и гемодинамической диагностики, возникает необходимость в выполнении зондирования полостей сердца и ангиокардиографии.
Лечение врожденных пороков сердца
Наиболее сложной проблемой в детской кардиологии является хирургическое лечение врожденных пороков сердца у детей первого года жизни. Большинство операций в раннем детском возрасте выполняется по поводу цианотических врожденных пороков сердца. При отсутствии у новорожденного признаков сердечной недостаточности, умеренной выраженности цианоза операция может быть отложена. Наблюдение за детьми с врожденными пороками сердца осуществляют кардиолог и кардиохирург .
Специфическое лечение в каждом конкретном случае зависит от разновидности и степени тяжести врожденного порока сердца. Операции при врожденных дефектах перегородок сердца (ДМЖП, ДМПП) могут включать пластику или ушивание перегородки , рентгенэндоваскулярную окклюзию дефекта . При наличии выраженной гипоксемии детям с врожденными пороками сердца первым этапом выполняется паллиативное вмешательство , предполагающее наложение различного рода межсистемных анастомозов. Подобная тактика улучшает оксигенацию крови, уменьшает риск осложнений, позволяет провести радикальную коррекцию в более благоприятных условиях. При аортальных пороках выполняется резекция или баллонная дилатация коарктации аорты, пластика аортального стеноза и др. При ОАП производится его перевязка. Лечение стеноза легочной артерии заключается в проведении открытой или эндоваскулярной вальвулопластики и т. д.
Анатомически сложные врожденные пороки сердца, при которых радикальная операция не представляется возможной, требуют выполнения гемодинамической коррекции, т. е. разделения артериального и венозного потоков крови без устранения анатомического дефекта. В этих случаях могут проводиться операции Фонтена , Сеннинга , Мастарда и др. Серьезные пороки, не поддающиеся оперативному лечению, требуют проведения пересадки сердца.
Консервативное лечение врожденных пороков сердца может включать в себя симптоматическую терапию одышечно-цианотических приступов, острой левожелудочковой недостаточности (сердечной астмы , отека легких), хронической сердечной недостаточности, ишемии миокарда, аритмий.
Прогноз и профилактика врожденных пороков сердца
В структуре смертности новорожденных врожденные пороки сердца занимают первое место. Без оказания квалифицированной кардиохирургической помощи в течение первого года жизни погибает 50-75% детей. В периоде компенсации (2-3 года) смертность снижается до 5%. Ранее выявление и коррекция врожденного порока сердца позволяет существенно улучшить прогноз.
Профилактика врожденных пороков сердца требует тщательного планирования беременности, исключения воздействия неблагоприятных факторов на плод, проведения медико-генетического консультирования и разъяснительной работы среди женщин групп риска по рождению детей с сердечной патологией, решения вопроса о пренатальной диагностике порока (УЗИ , биопсия хориона , амниоцентез) и показаниях к прерыванию беременности . Ведение беременности у женщин с врожденными пороками сердца требует повышенного внимания со стороны акушера-гинеколога и кардиолога.
Врожденные пороки сердца редко влияют на развитие плода. Впервые это было отмечено в исследованиях B. Mac Mahon и соавт. . Однако есть пороки, не совместимые с жизнью, и после рождения ребенок тотчас погибает. Некоторые врожденные пороки сердца, даже несложные формы, в раннем неонатальном периоде протекают злокачественно, обусловливая развитие декомпенсации кровообращения и дыхательную недостаточность. Главной причиной этого является несовершенство компенсаторных механизмов.
Диагностика у плода - одна из труднейших задач перинатологии. Многие врожденные пороки сердца, даже сложные, практически не совместимые с жизнью, антенатально не проявляются в силу особенностей внутрисердечной гемодинамики и после рождения становятся катастрофой для жизни ребенка.
Антенатальный период характеризуется особенностями кровообращения, такими как высокое давление в правом желудочке, незначительный объем кровотока в легочной артерии, параллельность работы желудочков сердца, функционирующие артериальный проток и овальное окно, нагнетающие кровь как обходные анастомозы в большой круг кровообращения за счет усиленной работы правого желудочка. Эти особенности внутрисердечной гемодинамики плода, безусловно, должны корректировать характер гемодинамических изменений ультразвуковых показателей сердца в норме и при пороках сердца у плода.
Известно, что у пациентов с врожденными пороками сердца нарушения гемодинамики в результате анатомических изменений в значительной степени влияют на данные ультразвукового сканирования сердца, такие как размеры полостей сердца, степень гипертрофии миокарда, функция клапанного аппарата, сократительная способность миокарда, направленность движения межжелудочковой перегородки.
Метод оценки внутрисердечной гемодинамики базируется на широко известных понятиях о систолической, объемной и смешанной перегрузках сердца, предложенных в 1952 г. E. Cabrera и J. Monroy .
В основе разделения использован следующий принцип.
Нагрузка сопротивлением возникает при ситуации, когда выброс крови из желудочков сердца в магистральные сосуды затруднен на уровне полулунных клапанов (стеноз аорты и легочной артерии), подклапанного пространства (идиопатический гипертрофический субаортальный стеноз, подклапанный стеноз аорты или легочной артерии), на протяжении сосудистого русла (коарктация аорты) либо при значительном увеличении выходного сопротивления (синдром Эйзенменгера). В результате затруднения выброса крови резко возрастает напряжение миокарда соответствующего желудочка при относительно стабильном объеме крови, что служит проявлением систолической перегрузки сердца. При систолической перегрузке желудочков сердца независимо от нозологической формы порока полость желудочка, несущего основную нагрузку сопротивлением, умеренно увеличивается в размерах. В ответ на нагрузку сопротивлением на эхокардиограмме выявляется гипертрофия миокарда соответствующего желудочка, и чем больше сопротивление выбросу, тем резче выражена степень гипертрофии миокарда соответствующего желудочка и межжелудочковой перегородки (рис. 1) .
Рис. 1. Систолическая перегрузка правого желудочка. Поперечное сечение желудочков сердца при стенозе легочной артерии. Градиент давления правый желудочек - легочная артерия равен 200 мм рт.ст. Выраженная гипертрофия межжелудочковой перегородки и миокарда передней стенки правого желудочка.
IVS - межжелудочковая перегородка, MRV - миокарда правого желудочка, RV - правый желудочек.
Нагрузка объемом возникает при дополнительном притоке крови в желудочки и в результате шунтирования крови через септальные перегородки или артериальный проток (дефекты межпредсердной и межжелудочковой перегородок, открытый артериальный проток), а также в результате обратного тока крови через атриовентрикулярные клапаны (клапанная недостаточность).
Характерными особенностями выраженной объемной перегрузки правого желудочка являются дилатация желудочка, при которой толщина миокарда не превышает верхней границы нормы, увеличение правого предсердия, парадоксальный характер движения межжелудочковой перегородки и увеличение амплитуды движения трикуспидального клапана (рис. 2, 3).
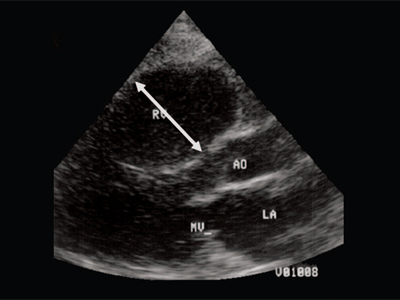
Рис. 2. Длинная ось сердца. Объемная перегрузка правого желудочка при дефекте межпредсердной перегородки. Объем сброса крови превышает 200% МОС. Отмечается выраженная дилатация правого желудочка.
RV - правый желудочек, AO - аорта, LA - левое предсердие, MV - митральный клапан.
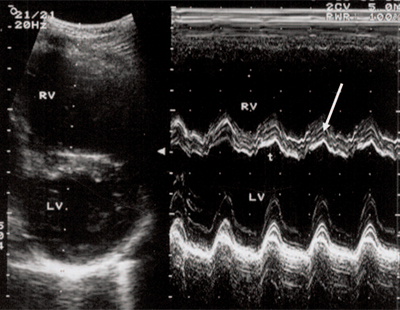
Рис. 3. Объемная перегрузка правого желудочка при дефекте межпредсердной перегородки. В- и М-сканирование. Стрелкой показан парадоксальный характер движения межжелудочковой перегородки.
Для левого желудочка признаком объемной перегрузки являются увеличение полости левого предсердия и желудочка, а также экскурсии межжелудочковой перегородки и миокарда задней стенки левого желудочка (рис. 4).
IVS - межжелудочковая перегородка, MLV - миокард левого желудочка, LV и RV - левый и правый желудочек.
При сочетании нагрузки сопротивлением и объемом возникает смешанная перегрузка (например, при дефекте межжелудочковой перегородки и повышении давления в легочной артерии для правого желудочка систолическая перегрузка сочетается с нагрузкой объемом, для левого желудочка в результате артериальновенозного сброса крови через дефект).
За многолетний период (с 1980 г. по настоящее время) наблюдений в ФГУ Научный центр акушерства, и перинатологии им. В.И. Кулакова Минздравсоцразвития России было замечено, что в антенатальном периоде не всегда работают принципы гемодинамических эхокардиографических проявлений врожденного порока сердца, которые ранее были разработаны и представлены в современной литературе .
Анализ более 2000 наблюдений врожденных пороков сердца у плода показал, что в ряде наблюдений имеются лишь анатомические изменения, характерные для определенной нозологической формы порока. При других врожденных пороках сердца изменения на эхокардиограмме связаны с характером гемодинамической нагрузки на сердце и аналогичны тому, что наблюдается после рождения. Наконец, в ряде наблюдений врожденных пороков сердца у плода вторичные изменения на эхокардиограмме, вызванные гемодинамическими нарушениями, отличаются от гемодинамических проявлений ультразвуковых показателей у детей и взрослых. Это позволило разделить все врожденные пороки сердца плода на три группы в зависимости от изменений на эхокардиограмме, обусловленных особенностями антенатальной внутрисердечной гемодинамики.
В первую группу вошли пороки сердца, которые, имея отчетливые анатомические проявления патологии, при ультразвуковом исследовании не имеют гемодинамических проявлений врожденного порока сердца. К ним относятся: дефект межпредсердной перегородки, дефект межжелудочковой перегородки, общий желудочек, простая форма транспозиции магистральных сосудов и также при наличии дефекта межжелудочковой перегородки общий артериальный ствол, двойное отхождение сосудов от желудочков сердца.
Следует это разобрать на примере дефекта межпредсердной перегородки. Основу расстройств внутрисердечной гемодинамики при дефекте межпредсердной перегородки составляет объемная перегрузка правых отделов сердца. При ультразвуковом исследовании у детей и взрослых это приводит к:
- дилатации правого желудочка (см. рис. 2, 3);
- увеличению правого предсердия;
- парадоксальному характеру движения межжелудочковой перегородки (см. рис. 2, 3).
Антенатально при равных величинах давления в желудочках сердца и в предсердиях объемной перегрузки не возникает. В связи с этим ни один из эхокардиографических гемодинамических признаков, используемых у детей и взрослых, не выявляется у плода. К эхокардиографическим проявлениям порока антенатально относится только прямой признак - перерыв ультразвукового луча в области дефекта. Размеры сердца, соотношение размеров желудочков сердца не отличаются от нормы (рис. 5).
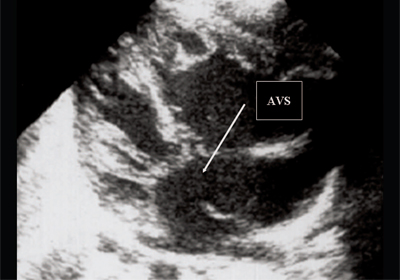
Рис. 5. Четырехкамерное сечение сердца плода. Стрелкой указан первичный дефект межпредсердной перегородки (АVS).
В равной степени это относится к дефекту межжелудочковой перегородки (рис. 6), простой форме транспозиции магистральных сосудов (рис. 7, 8), транспозиции магистральных сосудов с дефектом межжелудочковой перегородки (синдром Тауссиг - Бинга) (рис. 9), общему желудочку (рис. 10), общему артериальному стволу (рис. 10), двойному отхождению сосудов от одного из желудочков сердца (рис. 11).
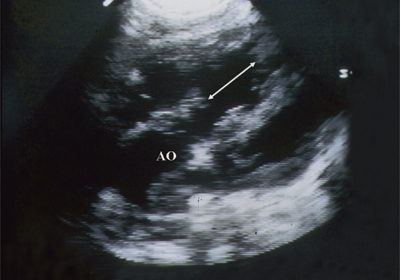
Рис. 6. Дефект межжелудочковой перегородки. Длинная ось сердца. Стрелками показан дефект межжелудочковой перегородки.
АО - аорта.
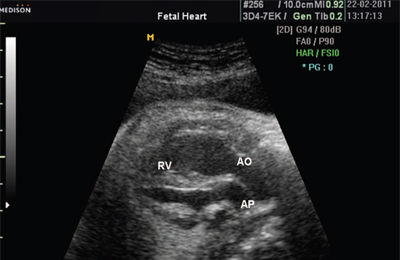
Рис. 7. Транспозиция магистральных сосудов.
АР - легочная артерия, АО - аорта, RV - правый желудочек.
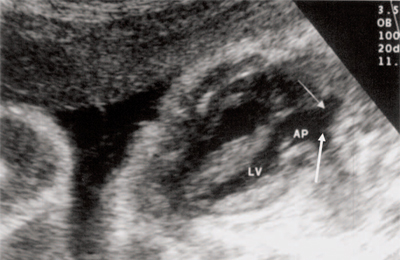
Рис. 8. Транспозиция магистральных сосудов, стрелками показаны ветви легочной артерии.
АР - легочная артерия, LV - левый желудочек.
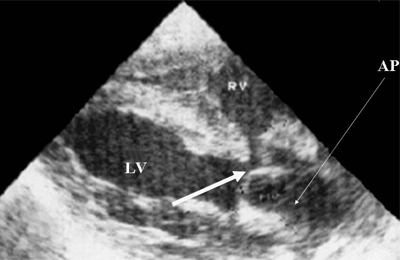
Рис. 9. Синдром Тауссиг - Бинга. Легочная артерия (отмечена стрелкой) расположена над дефектом межжелудочковой перегородки.
АР - легочная артерия, LV и RV - левый и правый желудочек.
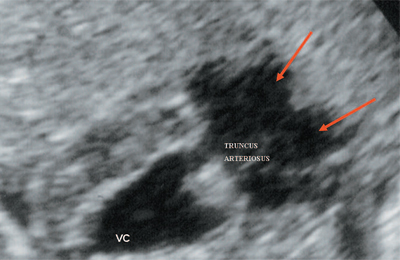
Рис. 10. Общий желудочек с отхождением TRUNCUS ARTERIOSUS. Стрелками показано разделение TRUNCUS ARTERIOSUS на аорту и ствол легочной артерии.
VC - общий желудочек, TRUNCUS ARTERIOSUS - общий артериальный ствол.
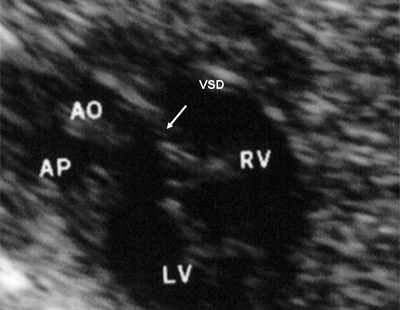
Рис. 11. Двойное отхождение магистральных сосудов от левого желудочка. Длинная ось сердца. Магистральные сосуды инвертированы и отходят от левого желудочка. Аорта расположена "верхом" над дефектом межжелудочковой перегородки (стрелка).
LV и RV - левый и правый желудочек, АР - легочная артерия, АО - аорта, VSD - дефект межжелудочковой перегородки.
Таким образом, диагностика перечисленных выше врожденных пороков сердца основывается на знании анатомических изменений, характерных для определенной нозологической формы патологии.
Вторая группа врожденных пороков сердца. При ультразвуковом исследовании регистрируются анатомические и гемодинамические изменения, характерные для определенной нозологической формы порока. В эту группу были отнесены: стеноз аорты, стеноз легочной артерии, врожденный митральный стеноз, транспозиция магистральных сосудов с сужением легочной артерии, обструкция опухолью выходного тракта одного из желудочков, аномалия Эбштейна, синдром гипоплазии правого и левого желудочков сердца, фиброэластоз, преждевременное закрытие овального окна.
Как пример можно разобрать изменения эхокардиографических показателей при клапанном стенозе легочной артерии. Нарушение гемодинамики при изолированном стенозе легочной артерии обусловлено препятствием на пути выброса крови в легочную артерию. Тяжесть стеноза определяется разницей систолического давления в правом желудочке и легочной артерии, т.е. градиентом давления.
При двухмерной выявляется утолщение створок клапана легочной артерии, экскурсия их уменьшена, а в систолу они образуют купол. Это анатомические проявления порока. К ним добавляются гемодинамические проявления: выраженная гипертрофия миокарда передней стенки правого желудочка и межжелудочковой перегородки, значительно превышающие нормативы. Степень выраженности гипертрофии миокарда правого желудочка зависит от степени стенозирования легочной артерии и соответственно от величины градиента давления. Эти данные получены при сопоставлении результатов ультразвукового сканирования и данных катетеризации полостей сердца у детей . Следует особо отметить, что при выраженной гипертрофии миокарда полость правого желудочка увеличивается незначительно. Отмечается также увеличение размера правого предсердия.
У плода получены аналогичные изменения, зависящие также от степени стенозирования легочной артерии. Полость правого желудочка, как видно на рис. 12, не увеличена. В то же время имеется значительная гипертрофия стенок правого желудочка. Как и в постнатальном периоде отмечено увеличение полости правого предсердия (рис. 13). После рождения при катетеризации полостей сердца в данном наблюдении был выявлен градиент давления на выходе из правого желудочка, равный 200 мм рт.ст.
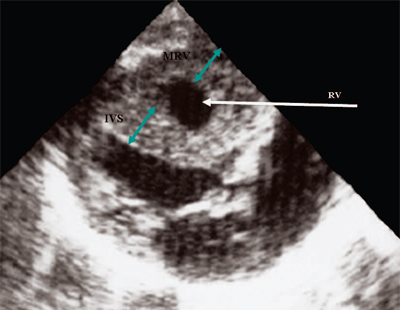
Рис. 12. Стеноз легочной артерии. Гипертрофия миокарда правого желудочка.
RV - правый желудочек, IVS - межжелудочковая перегородка, MRV - миокард правого желудочка.
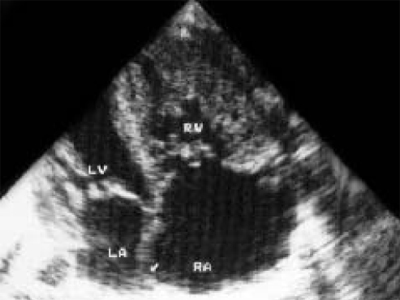
Рис. 13. Выраженный стеноз легочной артерии. Четырехкамерное сечение сердца. Значительное увеличение полости правого предсердия.
Такая взаимосвязь с нарушениями внутрисердечной гемодинамики у плода, безусловно, может быть выявлена лишь при выраженном нарушении оттока крови из правого желудочка в легочную артерию, ибо легочный кровоток в антенатальном периоде колеблется от 12 до 20%. Остальной объем крови поступает через артериальный проток в нисходящий отдел аорты. Поэтому незначительное стенозирование легочной артерии не столь информативно в плане гемодинамических ультразвуковых проявлений.
При аномалии Эбштейна антенатальная диагностика, как и в постнатальном периоде, базируется на определении области расположения трикуспидального клапана по отношению к митральному и смещении его вглубь правого желудочка. При исследовании обращают на себя внимание большие размеры сердца, преимущественно за счет правого предсердия (рис. 14). При допплеркардиографическом исследовании выявляется трикуспидальная недостаточность.
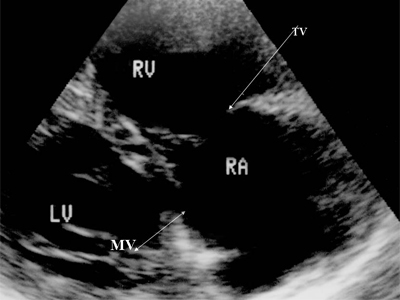
Рис. 14. Аномалия Эбштейна. Четырехкамерное сечение сердца. Отмечается смещение трикуспидального клапана к верхушке правого желудочка.
LV и RV - левый и правый желудочек, RA - правое предсердие, TV - трикуспидальный клапан, MV - митральный клапан.
Незначительное стенозирование аорты не вызывает нарушений гемодинамики у плода. При значительном препятствии выбросу крови из левого желудочка увеличивается величина давления в нем и усиливается работа левого желудочка. При выраженном стенозе значительно возрастает сопротивление выбросу крови, повышается также давление в левом предсердии и появляется лево-правый сброс крови через овальное окно в отличие от нормального для плода право-левого шунтирования. Это вызывает проявления сердечной недостаточности и может стать причиной внутриутробной задержки развития .
При ультразвуковом исследовании отмечается выраженная гипертрофия миокарда левого желудочка (рис. 15). Увеличивается размер левого предсердия. Может быть зарегистрирована митральная регургитация.
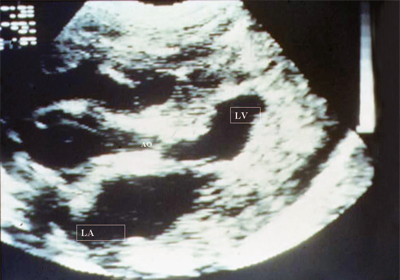
Рис. 15. Стеноз аорты. Длинная ось сердца. Отмечаются выраженное сужение аортального отверстия, выраженная гипертрофия миокарда левого желудочка, уменьшение его полости и дилатация левого предсердия.
LV - левый желудочек, LA - левое предсердие, АО - аорта.
При синдроме гипоплазии левых отделов нарушение кровообращения наступает на ранних стадиях развития плода. В отличие от нормального фетального кровообращения, когда кровь из полых вен частично проходит через овальное окно в левые отделы сердца и в большой круг кровообращения, вся кровь поступает в правый желудочек и легочный ствол. Отмечается также сброс крови из левого предсердия в правое через овальное окно . Поэтому антенатально отмечаются объемная перегрузка и дилатация правого желудочка (рис. 16). Особенностями внутрисердечной гемодинамики также объясняется то, что при цветном картировании потока выявляются ретроградный или двунаправленный кровоток через овальное отверстие и ретроградный кровоток в дистальном отделе аорты .
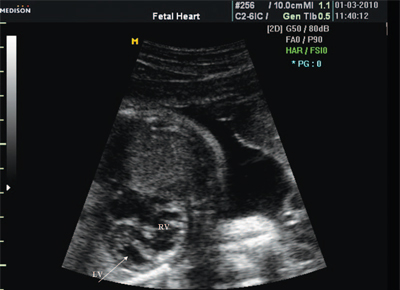
Рис. 16. Гипоплазия левого желудочка. Соотношение размеров полостей сердца изменено за счет компенсаторного увеличения размеров правого желудочка.
LV и RV - левый и правый желудочек.
Преждевременное закрытие овального окна. При антенатальном закрытии овального окна развивается правожелудочковая сердечная недостаточность и ребенок рождается обычно мертвым. Левые отделы становятся гипопластичными, миокард левого желудочка значительно гипертрофируется (рис. 17) .
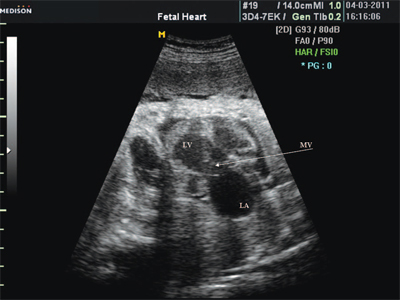
Рис. 17. Преждевременное закрытие клапана овального окна. Отмечаются умеренная гипоплазия левого желудочка, значительное увеличение левого предсердия, стрелкой показано митральное отверстие.
LV - левый желудочек, LA - левое предсердие, MV - митральный клапан.
Наконец, третья группа врожденных пороков сердца, которая по гемодинамическим изменениям эхокардиограммы антенатального периода отличается от изменений данных ультразвукового исследования в постнатальном периоде. Эта группа немногочисленна и будет подробно разобрана. В нее вошли следующие врожденные пороки сердца: атриовентрикулярный септальный дефект, тетрада Фалло, синдром Стейделя, коарктация аорты.
Атриовентрикулярный септальный дефект. При полной форме атриовентрикулярного септального дефекта все четыре камеры сообщаются между собой. Нарушения гемодинамики определяются наличием сообщений на предсердном и желудочковом уровнях и неполноценной функцией атриовентрикулярных клапанов. Нагрузка на все камеры сердца значительно увеличена.
Ультразвуковая диагностика атриовентрикулярного септального дефекта базируется на анатомических составляющих порока (выявление первичного дефекта межпредсердной перегородки; наличие высокого дефекта межжелудочковой перегородки; при полной форме наличие щели между митральным и трикуспидaльным клапаном). Имеются признаки аномалии митрального клапана, которые проявляются сближением передней створки с межжелудочковой перегородкой. Данный признак по аналогии с ангиографией носит название симптома "гусиной шеи" .
Кроме анатомических составляющих патологии, имеются изменения, связанныес гемодинамическими изменениями:
- увеличение правого предсердия;
- уменьшение размеров левого желудочка, связанное с наличием артериовенозного сброса крови, а также с часто наблюдаемой при атриовентрикулярном септальном дефекте умеренной гипоплазией левого желудочка.
Что же происходит антенатально? Кровь из верхней и нижней полых вен из правого предсердия через овальное окно поступает в левое предсердие. Поэтому увеличения правого предсердия, которое проявляется после рождения, у плода не отмечается. Имеется увеличение полости левого предсердия. Это первое отличие гемодинамических ультразвуковых признаков при атриовентрикулярном канале у плода (рис. 18).
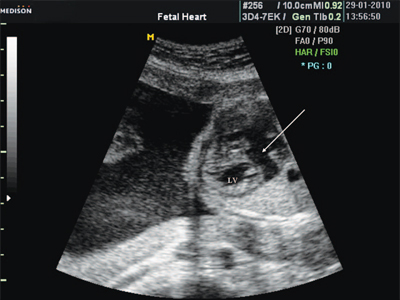
Рис. 18. Атриовентрикулярный септальный дефект (стрелка).
LV - левый желудочек.
Вторым отличием по гемодинамическим проявлениям являются увеличенные или нормальные размеры левого желудочка в отличие от уменьшенных размеров, наблюдаемых после рождения.
Тетрада Фалло. Гемодинамические изменения при тетраде Фалло обусловлены степенью препятствия выбросу крови из правого желудочка в малый круг кровообращения и наличием дефекта межжелудочковой перегородки. Величина сброса крови определяется степенью препятствия выбросу крови из правого желудочка в легочную артерию и сопротивлением большого круга кровообращения.
К анатомическим признакам патологии относятся декстропозиция аорты и дефект межжелудочковой перегородки. Отличительной особенностью при данной патологии считается увеличение диаметра аорты и инфундибулярное сужение легочной артерии. Гемодинамическим проявлением патологии следует считать гипертрофию миокарда правого желудочка при незначительном расширении его полости.
У плода также отчетливо визуализируются характерные анатомические изменения: широкая аорта, расположенная как "аорта-наездник", дефект межжелудочковой перегородки. В отличие от детей и взрослых инфундибулярный стеноз легочной артерии антенатально не выявляется. Отсутствие подклапанного сужения в раннем неонатальном периоде отмечают и патологоанатомы . Это соответствует мнению, что данная составляющая часть патологии проявляется в более зрелом возрасте и увеличивается с возрастом пациента .
Антенатально правый желудочек из-за наличия стеноза легочной артерии и дефекта межжелудочковой перегородки в работе сердца задействован меньше, чем это наблюдается в норме, когда основная нагрузка приходится именно на правые отделы сердца. Поэтому размер правого желудочка уменьшен по сравнению с нормой гестационного срока. В то же время кровообращение осуществляется за счет повышенной нагрузки на левый желудочек. Последний в результате усиленной работы гипертрофируется, начиная с 22-й недели гестации. Таким образом, для тетрады Фалло антенатально характерна гипертрофия миокарда левого желудочка (рис. 19) .
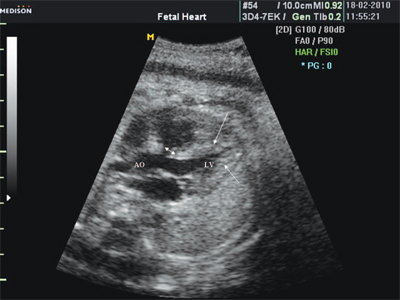
Рис. 19. Тетрада Фалло. Двойной стрелкой показан дефект межжелудочковой перегородки. Стрелками отмечена гипертрофия миокарда левого желудочка.
LV - левый желудочек, АО - аорта.
Коарктация аорты. Диагностическим основным признаком коарктации аорты является визуализация дуги и нисходящего отдела аорты с наличием анатомического ее сужения. Антенатально данный анатомический признак патологии наблюдается лишь в 30% наблюдений, так как коарктация часто формируется после рождения и закрытия артериального протока .
К гемодинамическим признакам порока у детей и взрослых относятся:
- гипертрофия миокарда левого желудочка;
- увеличение левого предсердия.
Антенатально при наличии коарктации аорты правый желудочек, активно участвующий в кровоснабжении органов плода, работает против сопротивления потоку через артериальный проток в нисходящий отдел аорты. В результате этого отмечаются увеличение полости правого желудочка и его гипертрофия. (рис. 20). Дилатируется также ствол легочной артерии. Данные ультразвуковые признаки патологии имеются в 70% наблюдений .
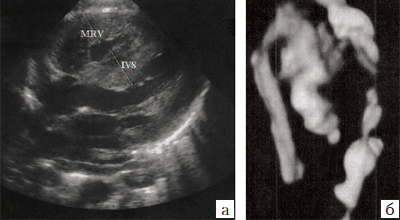
Рис. 20. Коарктация аорты (а, б). Выраженное сужение аорты в типичном месте в трехмерном изображении (б). При исследовании по длинной оси сердца отмечается выраженная гипертрофия миокарда правого желудочка.
MRV - миокард правого желудочка, IVS - межжелудочковая перегородка.
Была предложена оценка патологии по индексу отношения размера правого желудочка к размеру левого желудочка и отношения диаметра легочной артерии к диаметру аорты. В норме эти показатели соответственно равны 1,1 и 1,2.
При выраженном сужении аорты (сужение до 25% от нормальной величины) рано наблюдаются признаки сердечной недостаточности у плода, проявляющиеся наличием выпота в перикарде, значительным уменьшением размера левого желудочка и уменьшением величины сердечного выброса.
Гипоплазия левого желудочка с поражением дуг и аорты. Диагностика патологии антенатально, по мнению многих авторов, не представляет сложностей, все признаки, имеющие значение для диагностики у новорожденных и взрослых, должны быть использованы и при антенатальном исследовании.
К классическим ультразвуковым признакам синдрома гипоплазии левого желудочка относятся:
- резкое сужение восходящей дуги аорты;
- уменьшение конечно-диастолического размера левого желудочка;
- сужение диаметра аорты;
- увеличение конечно-диастолического размера правого желудочка;
- отношение конечно-диастолического размера левого желудочка к конечно-диастолическому размеру правого, равное или меньше 0,6;
- наличие грубых изменений митрального клапана.
Диагностическая задача может быть облегчена при наличии асцита, гидроперикарда у плода или при сопутствующей экстракардиальной патологии.
Выявление всех анатомических изменений при синдроме гипоплазии левого желудочка не представляет значительных трудностей. Однако имеющиеся наблюдения показали, что в некоторых случаях полость левого желудочка уменьшается незначительно, при этом имеется выраженная гипертрофия миокарда левого желудочка. Сопоставление с данными после рождения, а также с данными аутопсии показало, что такие не совсем характерные изменения при синдроме гипоплазии левого желудочка наблюдаются при наиболее тяжелой анатомической форме патологии - синдроме Стейделя (атрезии аортального клапана в сочетании с гипоплазией восходящего отдела аорты). Индекс отношения размера левого желудочка к размеру правого желудочка в диастолу находится в пределах 0,6. При гипоплазии левого желудочка без поражения дуги аорты он не превышает 0,15-0,2. При синдроме Стейделя, если имеются небольшие размеры левого желудочка, антенатально отмечается выраженная гипертрофия миокарда левого желудочка до 0,7 см (рис. 21), при синдроме гипоплазии левого желудочка без поражения дуги аорты толщина миокарда не превышает 2-3 мм .
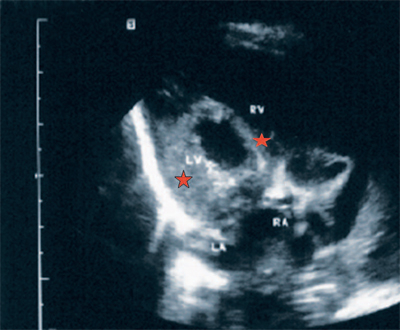
Рис. 21. Синдром Стейделя. Четырехкамерное сечение сердца. Полость левого желудочка уменьшена. Имеется выраженная гипертрофия миокарда левого желудочка и межжелудочковой перегородки. Полости правого желудочка и правого предсердия значительно увеличены в размерах.
LV и RV - левый и правый желудочек, LA и RA - левое и правое предсердие.
Таким образом, при многолетнем наблюдении пороков сердца у плода отмечены характерные особенности гемодинамических проявлений различных нозологических форм патологии. Все это с отчетливым проявлением анатомических составляющих пороков сердца может помочь в их антенатальной диагностике.
Литература
- Mac Mahon B., Mc Keown T., Record R.G. The incidence and life expectation of children with congenital heart disease // Br. Heart J. 1953. V. 15. P. 121-129
- Cabrera E., Monroy J. Systilic and Diastolic laging of the heart // Am. Heart J.1952. V. 43. N 5. P. 661.
- Затикян Е.П. Особенности внутрисердечной гемодинамики у больных врожденными пороками сердца при беременности. Дисс. ... докт. мед. наук. М., 1988.
- Бураковский В.И., Бокерия Л.А. Сердечно-сосудистая хирургия. М.: Медицина, 1989.
- Затикян Е.П. Гемодинамические закономерности изменений эхокардиограммы при врожденных пороках сердца // Кардиология. 1990. N 8. С. 47-50.
- Затикян Е.П. Врожденные и приобретенные пороки сердца у беременных. Функциональная и ультразвуковая диагностика. М.: Триада-Х, 2004.
- Allan L.D., Cook A.C., Huggon C. Fetal Echocardiography/ Cambridge University Press, 2009.
- Kleinmann C.S., Donnerstein R.L., De Vore G.R. et al. Fetal echocardiography for evalution of in utero congestive heart failure: A technique for study of nonimmune fetal hydrops // N. Engl. J. Med. 1982. V. 306. P. 568.
- Sahn D.J. Sh ndrome in utero associ ated with hydrops fetalis // Am. Heart J. 1982. V.104, N 6. P. 1368-1372.
- Norberger L.K., Sanders S.P., Rein A.J. et al. Left heart obstructive lesions and left ventricular growth in the midtrimester fetus. A longitudinale study // Circulation. 1995. V. 92. N 6. P. 1531-1538.
- Медведев М.В. Пренатальная эхография. Дифференциальный диагноз и прогноз. М.: Реал Тайм, 2009
- Nanda N., Gramiak R. Clinical Echocardiography. S. Louis, 1975.
- Zatikyan E.P. Atrioventricular septum defect in prenatal period // International Society The Fetus as a patient IX th International congress 1993. P. 41. Tokyo.
- Затикян Е.П. Атриовентрикулярный септальный дефект в пренатальном периоде // Ультразвуковая диагностика в акушерстве, гинекологии и педиатрии. 1993. N 3. C. 40-45.
- Ohba T., Matsui K., Nakamura K. et al. Tеtralogy of Fallot with absent pulmonary valve detected by fetal echocardiography // Int. Gynaecol. Obstet. 1990. V. 32. N 1. P. 71-74.
- Затикян Е.П. Кардиология плода. М.: Триада-Х, 2009.
- Allan L.D.,Chita S.K, Anderson R.H. et al. Coarctation of the aorta in prenatal life: and echocardiographic, anatomical and functional study // Br. Heart J. 1988. V. 59. P. 356.
- Затикян Е.П. Эхокардиографическая оценка выраженности анатомических и гемодинамических изменений при синдроме гипоплазии левых отделов сердца: динамическое наблюдение от плода к новорожденному // Ультразвуковая диагностика. 2000. N 3. С. 29-36.
Как известно, сердце - это важный орган в теле человека, от правильной его работы зависит благополучие всего организма. Сердце состоит из мышечной (миокард) и соединительной ткани (сердечные клапаны, стенки крупных сосудов). Деятельность сердца обусловлена ритмичным и последовательным сокращением составляющих его структур (предсердия и желудочки), в результате чего кровь, протекая через легкие, насыщается кислородом (так называемый малый круг кровообращения) и разносит кислород по всем органам и тканям (большой круг кровообращения).
Когда сердце плода развивается во время беременности, его работа отличается от работы сердца новорожденного ребенка и взрослого человека. В частности, малый круг кровообращения полноценно начинает функционировать только во время родов, когда происходит раскрытие легких новорожденного, и в момент первого крика они наполняются кровью. Поэтому в сердце плода существуют специальные отверстия и протоки, позволяющие циркулировать крови в формирующемся организме в обход легких (артериальный проток, соединяющий аорту и легочную артерию, овальное окно между предсердиями, венозный проток между пупочной веной и нижней полой веной).
Иногда под действием неблагоприятных факторов в период внутриутробного развития происходят грубые нарушения формирования анатомических структур сердца, что сказывается на его деятельности и не всегда совместимо с жизнью ребенка. Тогда либо по УЗИ плода во время беременности, либо в первые дни после родов новорожденному устанавливается диагноз врожденного порока развития сердца . Что это такое, каков прогноз для жизни и какие методы сохранения жизни и здоровья таких малышей предлагает современная медицина, мы и попробуем выяснить в данной статье.
Итак, эти патологические состояния представляют собой многочисленную группу заболеваний сердца, объединенных следующими признаками:
Возникают в период внутриутробного развития;
- характеризуются грубейшими нарушениями архитектоники сердца и крупных сосудов (аорта, нижняя и полая вена, легочные артерия и вены);
- анатомические изменения вызывают значительные нарушения в гемодинамике (циркуляции крови по организму);
- обусловлены недоразвитием анатомических структур или переменой их нормального расположения в сердце.
Частота распространенности варьирует от 6 до 9 на 1000 живых новорожденных. По данным разных авторов, возможных вариантов врожденных пороков развития сердца насчитывается от 50 до 100.
Схематичное изображение некоторых пороков сердца
Причины врожденных пороков сердца
В связи с тем, что во время внутриутробного развития происходит активное формирование всех органов человеческого организма, особенно сердца, плод и беременная женщина уязвимы к действию различных негативных факторов. Так, влияние на неправильное течение органогенеза могут оказать повышенный радиационный фон, ионизирующее излучение, инфекционные заболевания матери, особенно вирусные – краснуха, корь, ветрянка, герпес; прием некоторых лекарственных и токсических веществ (наркотиков, алкоголя) в период беременности, особенно в первом триместре (8 -12 –я недели – период наиболее интенсивного формирования всех органов плода). В 4 – 10% случаев врожденные пороки генетически обусловлены, то есть передаются по наследству.
Симптомы врожденных пороков сердца
Клиническая симптоматика пороков зависит от их вида. Выделяют пороки «синего» и «белого» типов, а также пороки, создающие препятствие кровотоку.
Основным проявлением «синих» пороков (транспозиция (перемена расположения) магистральных артерий, тетрада Фалло, атрезия – заращение - трикуспидального клапана) является цианоз – синее окрашивание кожи пальцев, кистей, стоп, носогубного треугольника, ушей, носа или, в крайне тяжелых случаях, всего тела. Также проявлением артериальной гипоксемии (пониженного содержания кислорода) являются одышка, потеря сознания с судорогами или без, тахикардия (учащенное сердцебиение), отставание в росте и развитии, частые простудные заболевания, неврологическая симптоматика в связи с отсутствием нормального кровоснабжения головного мозга. Как правило, пороки этого типа проявляют себя уже в первые часы и дни жизни новорожденного ребенка. Транспозиция магистральных артерий (полые вены входят в левое, а не правое предсердие, а аорта отходит от правого, а не левого желудочка) является тяжелым пороком, несовместимым с жизнью, и ребенок, как правило, погибает сразу после родов. Также к несовместимым с жизнью порокам относится трехкамерное сердце (два предсердия и один желудочек, или одно предсердие и два желудочка). Летальность пороков данного типа очень высока, если дети с такими пороками выживают в первые дни жизни, то без лечения погибают к концу первого – второго года.
К порокам белого типа
относятся дефект межжелудочковой перегородки, открытый Боталлов (артериальный) проток, дефект межпредсердной перегородки. Клинически эти пороки могут начать проявлять себя не в период раннего, детства, а к 16 – 20 годам. Симптомы пороков белого типа следующие: бледность кожных покровов, отставание в развитии, частые ОРВИ, признаки развивающейся правожелудочковой недостаточности – одышка и тахикардия при физической нагрузке или в покое.
Пороки с препятствием кровотоку: стеноз (сужение просвета) аорты, коарктация (сегментарное сужение) аорты, стеноз легочной артерии клинически проявляются одышкой, тахикардией, болями в грудной клетке, снижением выносливости, отеками, отставанием в развитии и нарушением кровообращения нижней половины туловища. При коарктации аорты дети доживают максимум до 2 –летнего возраста.
Диагностика врожденных пороков развития сердца
Как правило, диагностировать пороки развития плода, в том числе и сердца, возможно еще на этапе ультразвукового обследования беременной женщины. Тогда, в зависимости от вида порока, женщине может быть рекомендовано либо прерывание беременности (при пороках, не совместимых с жизнью, при множественных уродствах и т. д.), либо сохранение беременности с более детальным обследованием беременной и решением вопроса об оперативном лечении ребенка сразу или через некоторое время после родов. Но иногда в силу некоторых причин (не посещение беременной женской консультации и УЗИ кабинета, недостаточное оснащение фельдшерско-акушерских пунктов УЗИ аппаратурой и т. д.) пороки развития могут быть диагностированы только после родов.
Несмотря на то, что симптомы врожденных пороков достаточно яркие, в процессе клинического осмотра новорожденного ребенка диагноз можно только предположить, так как многие симптомы не являются строго специфичными, а могут быть обусловлены другими тяжелыми состояниями новорожденных (респираторный дистресс синдром, внутричерепные кровоизлияния и т. д.). Также не все пороки могут давать характерную аускультативную картину (в процессе выслушивания грудной клетки), и наоборот, шумы, щелчки или иные аускультативные проявления могут встречаться при незначительных отклонениях от нормы в строении сердца (малые аномалии). Поэтому, если порок сердца не был диагностирован по УЗИ плода, всем деткам с симптомами нарушения кровообращения (диффузный или акроцианоз, одышка при кормлении или в покое, потеря сознания, судороги), должно быть произведено УЗИ сердца во время пребывания в роддоме.
Эхокардиография (УЗИ сердца) это один из самых информативных методов визуализации пороков сердца. Также могут быть назначены ЭКГ (покажет нарушения ритма, гипертрофию предсердий и/или желудочков, если таковые имеются), рентгенография грудной клетки (покажет застой крови в легких, если есть, увеличение тени сердца в связи с расширением его камер). В особо сложных случаях или перед оперативным лечением могут быть назначены вентрикулография (введение рентгенконтрастного вещества в полость желудочков сердца), ангиография (введение контраста через сосуды в полости сердца), зондирование камер сердца с измерением в них давления.
Теперь остановимся подробнее на ультразвуковой диагностике часто встречающихся пороков сердца.
А. Врожденные порки сердца с объемной перегрузкой сосудов в легких (малого круга кровообращения).
1. Дефект межпредсердной перегородки - с помощью одномерной эхокардиографии выявляются признаки объемной перегрузки и дилатации (расширения) правого желудочка, при двухмерной эхокардиографии виден обрыв эхосигнала между предсердиями, а при допплер исследовании оценивается турбулентный (с «завихрениями») поток крови через межпредсердную перегородку и степень нарушений легочного кровотока.
2. Дефект межжелудочковой перегородки - при проведении УЗИ сердца визуализируются отверстие в перегородке между желудочками, дилатация левого и правого желудочков, турбулентный кровоток из левого в правый желудочек, оценивается степень тяжести легочной гипертензии, измеряется разница давления в желудочках.
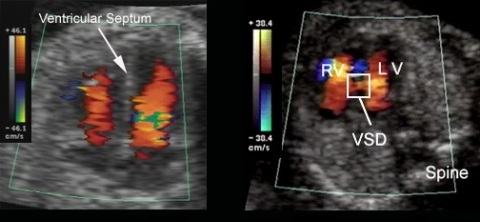
Так проявляется дефект перегородки между желудочками при проведении эхокардиографии с допплером. Слева - нормальная межжелудочковая перегородка, справа - ее дефект (VSD).
3. Открытый Боталлов проток – проявляется на эхокардиографии непрерывным кровотоком посредством сообщения в аорте и легочной артерии, изменением кровотока в устье легочного ствола.
4. Коарктация аорты – виден сегментарный участок сужения просвета аорты, ускоренный поток крови ниже сегмента.
5. Транспозиция магистральных артерий – визуализируется неправильное отхождение сосудов от сердца.
Б. Пороки сердца с уменьшением объема крови в малом круге кровообращения.
1. Тетрада Фалло – при эхокардиографии помимо стеноза (сужения) легочной артерии и дефекта перегородки между желудочками, определяется гипертрофия правого желудочка и отхождение аорты из правого желудочка, также оценивается степень нарушения внутрисердечной гемодинамики.
2. Стеноз легочной артерии – выявляется сужение просвета легочной артерии, и ускорение кровотока в устье легочной артерии и гипертрофия правого желудочка.
3. Аномалия Эпштейна – патология развития трехстворчатого клапана сердца, когда створки клапана прикрепляются не к фиброзному кольцу между предсердием и желудочком справа, а к стенкам правого желудочка, что вызывает уменьшение его объема. При ЭХО – КГ определяется патология клапана, оценивается степень расширения полостей сердца и нарушения внутрисердечного тока крови.
4. Атрезия трикуспидального клапана – при ЭХО – КГ отсутствует отражение эхосигнала от трикуспидального клапана, регистрируется гипертрофия правого предсердия и левого желудочка.
В. Пороки сердца с уменьшением объема циркулирующей крови в большом круге кровообращения (в сосудах всех жизненно важных органов).
1. Коарктация аорты (см. выше).
2. Изолированный стеноз аорты – оценивается степень сужения, визуализируется ускоренный кровоток через аортальный клапан и деформированные створки клапана.
Г. Пороки сердца без нарушения гемодинамики.
- Декстрокардия (зеркальное расположение сердца справа) – достаточно редкая аномалия, по УЗИ сердца нарушений гемодинамики, как правило, не регистрируется.
Лечение врожденных пороков развития сердца
Полное излечение подавляющего большинства пороков сердца возможно только с помощью их хирургической коррекции. Кардиохирургические операции могут быть проведены в первые часы или дни жизни новорожденного, либо на первом году жизни ребенка. При открытом артериальном протоке допустима выжидательная тактика (при отсутствии симптомов жизнеугрожающих состояний), так как этот проток может самостоятельно закрываться в первые два года жизни.
Операции могут выполняться как на открытом сердце (с рассечением стенки грудной клетки), так и кардиоваскулярным методом (когда доступ к сердцу осуществляется посредством введения в сосуды зонда, достигающего полостей сердца). Последний метод, например, применяется при коррекции дефектов между предсердиями или желудочками, к которым с помощью зонда подводится окклюдер, закрывающий отверстия.
Но при некоторых пороках сердца, не совместимых с жизнью, например, трехкамерное сердце (одно предсердие и два желудочка, или два предсердия и один желудочек) проведение хирургической коррекции, к сожалению, не возможно.
Кроме кардиохирургической операции, пациенту назначается медикаментозная терапия для улучшения сократительной функции сердца и «разгрузки» малого круга кровообращения. Применяются ингибиторы АПФ (эналаприл, периндоприл, лизиноприл, рамиприл и др), диуретики (фуросемид, индапамид и др), В-адреноблокаторы (карведилол, бисопролол и др).
Образ жизни с врожденным пороком сердца
Пациенту необходимо соблюдать следующие рекомендации относительно его образа жизни:
- рациональное сбалансированное питание;
- соблюдение диеты с ограничением поваренной соли и объема потребляемой жидкости (для уменьшения объемной перегрузки сердца и сосудов);
- достаточное пребывание на свежем воздухе;
- исключение любых занятий спортом и ограничение сильных физических нагрузок;
- достаточный по продолжительности сон;
- регулярное наблюдение у кардиолога и кардиохирурга с проведением необходимых лечебно-диагностических мероприятий;
- беременность женщинам с пороками «синего» типа строго противопоказана, но если было проведено хирургическое лечение, то возможность сохранения беременности определяется в каждом конкретном случае индивидуально с совместным ведением беременной кардиохирургом, кардиологом и акушер-гинекологом в специализированном стационаре. Родоразрешение, как правило, проводится путем кесарева сечения.
Прогноз при врожденных пороках сердца
Прогноз для жизни большинства пороков сердца неблагоприятный. Как уже было сказано выше, кардиохирургическое лечение таким деткам требуется в первые дни и месяцы после родов, иначе они погибают в течение первых двух лет из–за прогрессирования сердечной недостаточности или присоединения осложнений (бактериальный эндокардит, фатальные нарушения ритма, повышенный риск тромбообразования и тромбоэмболических осложнений, частые заболевания бронхолегочной системы (затяжные бронхиты, тяжелые пневмонии). Исключение составляют пороки белого типа, при которых в случае отсутствия хирургического лечения в силу каких либо причин дети способны доживать до 16 – 18 лет.
После хирургической коррекции прогноз для жизни благоприятный, но все равно состояние ребенка остается достаточно серьезным, поэтому за такими детьми должно осуществляться усиленное наблюдение родителей и врачей.
В заключение хотелось бы отметить, что данный диагноз у ребенка на современном этапе развития медицины не является приговором, так как возможности отечественной и зарубежной кардиологии детского возраста позволяют выносить, родить и вырастить малыша, способного вести полноценный образ жизни, несмотря на столь тяжелое заболевание.
Врач терапевт Сазыкина О.Ю.
Каждая беременная женщина испытывает море положительных и волнительных эмоций, в ожидании будущего малыша. Но у такого волнительного состояния, как женская беременность есть и другая сторона медали. Казалось бы, что может быть не так с ожиданием появления ребенка. К сожалению, различные патологии добавляют горечи в ситуацию с беременностью. Особенно много проблем во время вынашивания плода будущие мамочки испытывают в наше время.
Из всех возможных проблем, возникающих при вынашивании плода, одними из самых тревожных болезней считаются болезни сердечно-сосудистой системы. Среди рожениц нередко встречаются женщины с различными сердечными пороками. Бывают случаи, когда болезни сердца касаются и вынашиваемого плода. Врожденный сердечный порок - довольно-таки серьезная проблема, которая приводит к многим нежелательным последствия и заметному ухудшению состояния здоровья ребенка.
Порок сердца у плода, чаще всего, появляется из-за некоторых нарушений развития внутри утроба матери. Симптомы заболевания возможно обнаружатся сразу после родов, но иногда признаки врожденной сердечной патологии протекают крайне вяло, почти никак себя не выдавая. Хотя, своевременная диагностика и обследования малыша - позволят определить наличие имеющейся патологии.
Основополагающими факторами возникновения патологии у будущего ребенка, касающегося сердечного органа, могут быть некоторые причины, на которые на необходимо обратить свое внимание в первую очередь:
1 Генетическая предрасположенность - данное заболевание нередко может передаться генетическим способом. Это ответ для тех, кто интересуется передается ли сердечный порок по наследству. К сожалению, подобные патологии имеют отличительные черту - они нередко передаются от родителей к детям. Что примечательно, заболевание передается в основном по материнской линии. Если у матери имеются болезни сердца, то риск подобной патологии у будущего малыша увеличивается почти в восемь раз.
Порок сердца у беременных может стать нешуточной проблемой, при родах или вынашивании плода, как для самой будущей матери, так и для еще не появившегося на свет младенца. Учитывая, то обстоятельство, что порок сердца по-наследству передается очень часто, стоит перед планированием беременности либо излечиться от недуга, либо всеми способами постараться предотвратить передачу патологии будущему ребенку.

2 Неблагоприятное влияние некоторых внешних факторов - загрязненность окружающей среды из-за выбросов радиоактивных отходов, да и вообще, любой контакт с химикатами чреват риском развития рассматриваемой патологии у вынашиваемого плода. Помимо этого, следует отметить, что беременным женщинам не стоит проводить раннюю рентгенографию. Рентгеновское исследование при вынашивании плода, даже единичное, способно вызвать нежелательные отклонения. Рентгенографию можно применить только после двенадцатой недели беременности, раньше этого срока не рекомендуется.
3 Некоторые хронические заболевания матери - наиболее неблагоприятной, а также опасной патологией является сахарный диабет второго типа (инсулинозависимый сахарный диабет). Такое тяжелое заболевание часто оканчивается незапланированным срывом беременности. На вопрос можно ли рожать при инсулинозависимом сахарном диабете, многие опытные медики ответят, что делать этого не стоит. Чаще всего, такая патология приводит к катастрофическим последствиям,ставя под угрозу и жизнь роженицы, и здоровье будущего малыша.
В случаях, когда беременная женщина хочет рожать, несмотря ни на какие уговоры врачей и близких, возможно воспользоваться искусственным родоразрешением. Однако, ребенок после родов появится на свет очень слабым, даже недоразвитым. Таким детям важен тщательный уход под контролем опытных медиков, иначе, а так часто бывает на практике, ребенок может умереть.
4 Длительное употребление различных медикаментозных средств - некоторые виды лекарственных средств, типа антибиотиков или транквилизаторов способны создать условия, способствующие гормональным нарушения в организме женщины. Этот фактор потом отражается на здоровье будущего малыша, что нередко способствует появлению у вынашиваемого плода порока сердца.
5 Патологии инфекционного характера - некоторые из вирусных заболеваний по своей природе могут протекать незаметно для зараженной будущей мамы. По этой причине, до планирования беременности, стоит тщательно провериться на наличие инфекционных заболеваний.
6 Пристрастие к пагубным привычкам - наличие вредоносных для организма привычек не красит женщину, и к тому же такое рьяное увлечения курением либо распиванием спиртных напитков часто сказывается на здоровье вынашиваемого плода. Курить, пить, принимать наркотические средства: до беременности не рекомендуется, а во время вынашивания будущего ребенка - категорически запрещено.
Пороки сердца и беременность при таких патологиях очень несовместимые вещи. При планировании беременности будущим мамочкам стоит полностью отказаться от вредных привычек, провериться на наличие инфекционных болезней. Такие меры предосторожности помогут снизить риск появления у будущего ребенка врожденных патологий сердца.
Порок сердца у вынашиваемого плода при беременности и как его определить
Современная медицина насчитывает огромное многообразие различных сердечных пороков. По последним данным, в нынешнее время существуют около ста разновидностей порока сердца. Следует отметить, что порок сердца - это заболевание, которое сказывается на работе сердца. При этой болезни, сам орган, точнее его составные части, несколько видоизменены. Дисфункция сердечных клапанов, как правило, является основной причиной, влекущей за собой различные пороки сердца.

Из-за изменений сердечной структуры происходит процесс нарушения кровообращения. При этом орган не может поставлять кислород, в достаточном количестве, к органам и тканям организма. Порок сердца, в связи с этим неприятным явлением, особенно опасен для здоровья беременной женщины, которая, как никогда нуждается в самой важной функции сердечного органа - поставкой кислорода к органам тела и мышечным тканям. Но рожать с пороком сердца можно, вот только необходимо знать симптомы заболевание, если вдруг будущий малыш появится на свет с врожденной сердечной патологией.
Но узнать, приобрел ли вынашиваемый плод пороки сердца или нет возможно еще до его рождения. Благо, современная медицина обладает подобными возможностями. Правда, единственный способ проверить состояние здоровья ребенка в утробе матери - это обследование с помощью ультразвука. Ультразвуковое обследование пациентки при беременности, целесообразно проводить, начиная с семнадцатой недели вынашивания плода. Процедуру надо повторять вплоть до двадцатой недели беременности.
Метод ультразвукового исследования будущих мамочек, считается достаточно сложным. Этот способ диагностики требует новейшего медицинского оборудования, а также высококвалифицированного специалиста, который сможет дать точный анализ происходящему.
Если, все же у плода выявили наличие порока сердца, то врачи должны предпринять все необходимые меры для сохранения беременности, а также стараться спасти жизнь будущему малышу. Вообще при таком печальном диагнозе, беременной женщине должны сделать повторное ультразвуковое исследование, но только по истечении определенного времени (на более поздних стадиях вынашивания плода). Начиная с седьмого месяца беременности, можно проводить эхокардиографию пациентки, чтобы получить больше сведений о заболевании.
При выявлении порока сердца у плода, в наше время, имеются возможности повлиять на благополучный исход родоразрешения. При рождении малыша, с сердечной патологией, его должны обследовать опытные врачи. Обычно дети рожденные с пороками сердца подключаются к аппаратам искусственного кровообращения. Делается это, для проведения хирургической операции, которая позволяет устранить причины недуга. В некоторых случаях может понадобиться более одной операции - все зависит от степени тяжести заболевания.
Пороки сердца у беременной, какие бывают виды недуга?
Порок сердца для будущей матери становится тяжелой проблемой. Современная медицина различает несколько наиболее встречающихся видов этого недуга. Вместе с тем, надо отметить, что заболевание носит либо врожденный, либо приобретенный характер. Врожденные пороки сердца делятся на три основные группы, которые подробно стоит рассмотреть, чтобы иметь полное представление об угрозе, таящейся за болезнью:
1 Циркуляция крови от левого предсердия к правому - очень тяжелая форма недуга, при которой вынашивание плода чревато критическими последствиями. Если у беременной зафиксирован подобный диагноз, то необходимо прервать процесс вынашивания плода. Игнорирование этой процедуры может стать причиной летального исхода будущей матери. Происходит такое - из-за того, что сердечный орган испытывает непосильные нагрузки, вследствие нарушения процесса кровообращения

2 Сужение сосудов кровеносной системы или стеноз сосудов - такой диагноз для будущей мамочки не так опасен, как предыдущий. Родить при стенозе сосудов вполне реально, но возможно пациентке необходимо будет сделать кесарево сечение.
3 Самыми популярными патологиями врожденного порока сердца - являются болезни, при которых наблюдается циркуляция крови от правого предсердия к левому. К данным заболеваниям относятся отклонения, касающиеся межжелудочковой, а также межпредсердной перегородок. В случаях, когда патология переходит в сердечную недостаточность, медики рекомендуют прервать беременность. Но, если женщина настаивает на родах, то шанс благополучного исхода родоразрешения имеется. Под наблюдением опытных докторов, даже с таким диагнозом, как сердечная недостаточность возможно родить вполне здорового ребенка.
Если говорить о приобретенных пороках, то причин, благоприятствующих их появлению множество. Приобретенные пороки сердца - не зря называют клапанными пороками. При таком виде недуга происходит дисфункция сердечных клапанов. Клапаны, как правило, анормального строения, потому не справляются со своими задачами в процессе кровоснабжения организма. Среди самых распространенных факторов, из-за которых приобретаются различные пороки сердца, наиболее распространены следующие:
- Приобретенный порок сердца часто становится следствие перенесения такого венерического заболевания, как сифилис. Если будущая мамочка, когда-то болела сифилисом, то ей необходимо тщательно подготовиться к беременности и проконсультироваться с опытными специалистами, чтобы развеять все сомнения, касающиеся процесса вынашивания плода, родоразрешения.
- Воспаление соединительных тканей сердечно-сосудистой системы (ревматизм) - одна из основных причин приобретенного порока сердца. Данная патология может потревожить пациентку сильными болями в области груди, одышкой, учащенным пульсом.

- Часто причинами приобретенных пороков сердца становятся такие сердечные патологии, как ишемическая болезнь сердца и гипертония.
- Различные травмы грудной клетки приводит к повреждения внутримышечных тканей сердца, что способствует развитию сердечных заболеваний.
- Атеросклероз сердечных сосудов - опасная патология, которая приводит к сужению сосудов сердечного органа, вследствие чего нарушается кровообращение. Большое количество пороков сердца приобретаются именно из-за атеросклероза.
- Гибель сердечных клеток под влиянием воспалительного процесса (кардиосклероз) - также относится к одной из вероятных причин приобретенного порока сердца у беременной пациентки.
Кроме того, что будущая мать, если она больна пороком сердца, может передать данный недуг еще не родившему ребенку, есть и другие неблагоприятные факторы, влияющие на здоровье малыша внутри материнской утробы. Например, порок сердца при беременности часто приводит к гипоксии плода. Данное явление очень опасно для состояния здоровья вынашиваемого ребенка. Такое состояние, как гипоксия плода приводит к кислородному голоданию плода, а этот процесс нередко становится причиной многих врожденных патологий.



